EA 575® - Dịch chiết cao khô lá thường xuân

Quá trình nghiên cứu

Vì sao EA 575® khác biệt?
chuẩn hóa
chuẩn hóa
ổn định & chuẩn hóa
α-hederin, β-hederin, hederacoside C… - nền tảng tạo nên 4 cơ chế tác động toàn diện.
Cơ chế tác dụng 4-trong-1
của EA 575®
Thành phần hoạt chất: Chiết xuất khô lá thường xuân EA 575®
Nhóm thuốc: Thuốc long đờm

CƠ CHẾ LONG ĐỜM
- Đối tượng: 24 trẻ em (4-12 tuổi) bị hen phế quản.
- Thời gian điều trị: 3 ngày với EA 575® hoặc giả dược.
- Mục tiêu: Đánh giá tác dụng của EA 575® trong việc giảm sức cản đường thở (RAW) ở trẻ bị co thắt phế quản.
- Loại nghiên cứu: Nghiên cứu lâm sàng đối chứng chéo, ngẫu nhiên, mù đôi.
(2) Nghiên cứu tiền lâm sàng về tác dụng chống viêm của EA 575® – Schulte-Michels et al., 2016
- Đối tượng: Mô hình tế bào miễn dịch viêm (macrophages) trong phòng thí nghiệm.
- Thời gian nghiên cứu: Ngắn hạn - đánh giá phản ứng viêm cấp.
- Mục tiêu: Kiểm tra khả năng EA 575® làm giảm sản xuất các chất trung gian gây viêm, đặc biệt là IL-6.
- Loại nghiên cứu: Nghiên cứu tiền lâm sàng (in vitro), sử dụng mô hình tế bào được kích hoạt viêm bằng LPS.
Giúp giảm khó thở, cải thiện hô hấp nhanh chóng.
giúp giãn đường thở và cải thiện lưu thông khí.
CƠ CHẾ GIÃN PHẾ QUẢN
- Đối tượng: 24 trẻ em (4-12 tuổi) bị hen phế quản.
- Thời gian điều trị: 3 ngày với EA 575® hoặc giả dược.
- Mục tiêu: Đánh giá tác dụng của EA 575® trong việc giảm sức cản đường thở (RAW) ở trẻ bị co thắt phế quản.
- Loại nghiên cứu: Nghiên cứu lâm sàng đối chứng chéo, ngẫu nhiên, mù đôi.
Giúp giảm khó thở, cải thiện hô hấp nhanh chóng.
CƠ CHẾ CHỐNG VIÊM
- Đối tượng: 24 trẻ em (4-12 tuổi) bị hen phế quản.
- Thời gian điều trị: 3 ngày với EA 575® hoặc giả dược.
- Mục tiêu: Đánh giá tác dụng của EA 575® trong việc giảm sức cản đường thở (RAW) ở trẻ bị co thắt phế quản.
- Loại nghiên cứu: Nghiên cứu lâm sàng đối chứng chéo, ngẫu nhiên, mù đôi.
(2) Nghiên cứu tiền lâm sàng về tác dụng chống viêm của EA 575® – Schulte-Michels et al., 2016
- Đối tượng: Mô hình tế bào miễn dịch viêm (macrophages) trong phòng thí nghiệm.
- Thời gian nghiên cứu: Ngắn hạn - đánh giá phản ứng viêm cấp.
- Mục tiêu: Kiểm tra khả năng EA 575® làm giảm sản xuất các chất trung gian gây viêm, đặc biệt là IL-6.
- Loại nghiên cứu: Nghiên cứu tiền lâm sàng (in vitro), sử dụng mô hình tế bào được kích hoạt viêm bằng LPS.
Giúp giảm khó thở, cải thiện hô hấp nhanh chóng.
CƠ CHẾ GIẢM HO
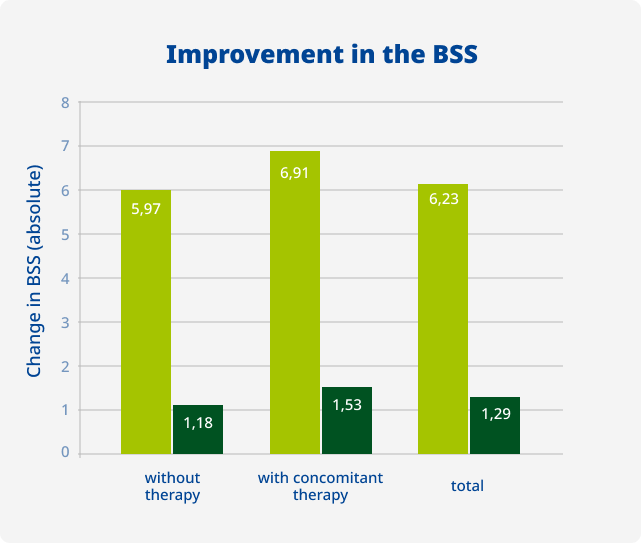
- Đối tượng: 1.066 trẻ em (6–12 tuổi) bị viêm phế quản cấp.
- Thời gian điều trị: 7 ngày với các dạng bào chế khác nhau của EA 575® (siro, viên ngậm, viên sủi…).
- Mục tiêu: Đánh giá hiệu quả giảm ho, giảm số lần thức giấc ban đêm và khả năng dung nạp thuốc ở trẻ.
- Loại nghiên cứu: Nghiên cứu tiến cứu, không can thiệp, đa trung tâm
Giảm 71% số lần thức giấc ban đêm do ho (từ ~7 lần xuống còn 2 lần).
EA 575®- 4 Cơ chế hợp lực
tạo hiệu quả tốt

-
Loãng đờmĐờm dễ tống xuất, giảm bít tắc đường thở
-
Chống viêmGiảm sưng đỏ, giảm kích ứng gây ho
-
Giãn phế quảnĐường thở mở rộng, hít thở dễ dàng hơn
-
Giảm hoDịu họng, cải thiện giấc ngủ



Không chất tạo màu
Engelhard Arzneimittel - thương hiệu toàn cầu, nơi EA 575® ra đời
Chính tại đây, EA 575® - dịch chiết khô từ lá Thường xuân - được tạo ra bằng quy trình chiết xuất chuẩn hóa, đảm bảo hàm lượng hoạt chất ổn định và chất lượng đồng nhất trên toàn thế giới.
Tài liệu tham khảo
(1) Lang, Christopher et al. “A Valuable Option for the Treatment of Respiratory Diseases: Review on the Clinical Evidence of the Ivy Leaves Dry Extract EA 575®.** Planta medica vol. 81,12-13 (2015): 968-74.
(2) Völp, Andreas et al. “Ivy leaves extract EA 575 in the treatment of cough during acute respiratory tract infections: meta-analysis of double-blind, randomized, placebo-controlled trials.” Scientific reports vol. 12,1 20041. 21 Nov. 2022
(3) Shekelle, P G et al. “Clinical guidelines: developing guidelines.” BMJ (Clinical research ed.) vol. 318,7183 (1999): 593-6.
(4) Schaefer, A et al. “A randomized, controlled, double-blind, multi-center trial to evaluate the efficacy and safety of a liquid containing ivy leaves dry extract (EA 575®) vs. placebo in the treatment of adults with acute cough.” Die Pharmazie vol. 71,9 (2016): 504-509.
(5) Schaefer, Axel et al. “Efficacy of two dosing schemes of a liquid containing ivy leaves dry extract EA 575 versus placebo in the treatment of acute bronchitis in adults.” ERJ open research vol. 5,4 00019-2019. 8 Dec. 2019.
(6) Meurer, Fabio et al. “Ivy leaves dry extract EA 575® mediates biased β2-adrenergic receptor signaling.” Phytomedicine : international journal of phytotherapy and phytopharmacology vol. 90 (2021): 153645.
(7) R. Gonzales, M. A. Sande, Uncomplicated acute bronchitis. Ann Intern Med 133, 981-991 (2000).
(8) G. Worrall, Acute bronchitis. Can Fam Physician 54, 238-239 (2008).
(9) J. V. Fahy, F. B. Dickey, Airway mucus function and dysfunction. N Engl J Med 363, 2233-2247 (2010).
(10) M. Bailey, H. Engler, J. Hunzeker, J. F. Sheridan, The hypothalamic-pituitary-adrenal axis and viral infection. Viral Immunol 16, 141-157 (2003).
(11) S. E. Calvano, S. M. Coyle, Experimental human endotoxemia: a model of the systemic inflammatory response syndrome? Surg Infect (Larchmt) 13, 293-299 (2012).
(12) M. A. Giembycz, R. Newton, Beyond the dogma: novel beta2-adrenoceptor signalling in the airways. Eur Respir J 27, 1286-1306 (2006).
(13) S. A. Rooney, Regulation of surfactant secretion. Comp Biochem Physiol A Mol Integr Physiol 129, 233-243 (2001).
(14) J. Hohlfeld, H. Fabel, H. Hamm, The role of pulmonary surfactant in obstructive airways disease. European Respiratory Journal 10, 482-491 (1997).
(15) A. Anzueto et al., Effects of aerosolized surfactant in patients with stable chronic bronchitis: a prospective randomized controlled trial. Jama 278, 1426-1431 (1997).
(16) C. A. Moore, S. K. Milano, J. L. Benovic, Regulation of receptor trafficking by GRKs and arrestins. Annu Rev Physiol 69, 451-482 (2007).
(17) P. E. Moore et al., Respiratory syncytial virus infection reduces beta2-adrenergic responses in human airway smooth muscle. Am J Respir Cell Mol Biol 35, 559-564 (2006).
(18) A. Sieben et al., α-Hederin, but not hederacoside C and hederagenin from Hedera helix, affects the binding behavior, dynamics, and regulation of β2-adrenergic receptors. Biochemistry 48, 3477-3482 (2009).
(19) J. Schulte-Michels et al., α-Hederin inhibits G protein-coupled receptor kinase 2-mediated phosphorylation of β2-adrenergic receptors. Phytomedicine 23, 52-57 (2016).
(20) H. Bussmann et al., A comparative study of the influence of an ivy preparation and an ivy/thyme combination on the beta2-adrenergic signal transduction. Heliyon 6, e03960 (2020).
(21) J. Schulte-Michels, F. Runkel, S. Gokorsch, H. Häberlein, Ivy leaves dry extract EA 575® decreases LPS-induced IL-6 release from murine macrophages. Die Pharmazie-An International Journal of Pharmaceutical Sciences 71, 158-161 (2016).
(22) J. Schulte-Michels, C. Keksel, H. Haberlein, S. Franken, Anti-inflammatory effects of ivy leaves dry extract: influence on transcriptional activity of NFkappaB. Inflammopharmacology 27, 339-347 (2019).
(23) A. E. McGovern, K. R. Short, A. A. Kywe Moe, S. B. Mazzone, Translational review: Neuroimmune mechanisms in cough and emerging therapeutic targets. J Allergy Clin Immunol 142, 1392-1402 (2018).
(24) Kraft, K “Verträglichkeit von Efeublättertrockenextrakt im Kindesalter” Zeitschrift für Phytotherapie 2004; 25: 179-181.
(25) Fazio, S. et al. “Tolerance, safety and efficacy of Hedera helix extract in inflammatory bronchial diseases under clinical practice conditions: a prospective, open, multicenter postmarketing study in 9657 patients.” Phytomedicine 2009, 16, 17-24.





